ENLACE COVALENTE
-ES LA UNION ENTRE EN LA QUE SE COMPARTEN LOS ELECTRONES DE ENLACE PARA LOGRAR LA MAYOR ESTABILIDAD (FORMANDO UN OCTELO ENTRE LOS 2).
EXISTEN 3 TIPOS DE ENLACES COVALENTES:
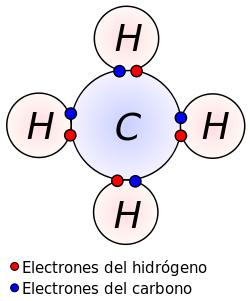
ENLACE COVALENTE APOLAR :
-OCURRE CUANDO LA DIFERENCIA DE ELECTRONEGATIVIDAD ES MUY CERCANA A CERO .
-LOS ELECTRONES DEL ENLACE ESTAN EQUIDISTANTE DE AMBOS ATOMOS , ES DECIR COMPARTEN POR IGUAL.
- GENERALMENTE SE DA ENTRE ATOMOS DE UN MISMO ELEMENTO , O BIEN ENTRE ATOMOS CUYA ELECTRONEGATIVIDAD ES MUY CERCANA.
EJEMPLO:
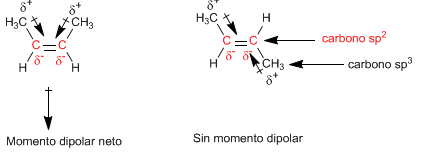
MOMENTO DIPOLAR:
- ES UN VECTOR ( MODULO, DIRECCION Y SENTIDO)
- SE DETERMINA DE MANERA GLOBAL
- SON MOLECULAS CUYOS ENLACES SEAN COVALENTES POPULARES , PUEDEN TENER UN MOMENTO DIPOLAR NULO.
- LAS MOLECULAS CUYOS ENLACES SEAN EXCLUSIVAMENTE APOLARES TENDRAN UN MOMENTO DIPOLAR NULO.
ENLACE COVALENTE POLAR
- SE CARACTERIZA PORQUE LOS ELECTRONES DE ENLACES ES COMPARTIDO POR AMBOS ATOMOS DE MANERA DESIGUAL.
- UNO DE LOS ATOMOS ( EL MAS ELECTRONEGATIVO) ATRAE MAS HACIA SI LOS ELECTRONES DE ENLACE, MAS NO LOGRA DESPRNDERLOS DEL TODO COMO EN EL IONICO.
- OCURRE CUANDO LA DIFERNCIA DE ELECTRONEGATIVIDAD ES MENOR QUE 1.7 PERO MAYOR QUE 0.1.
EJEMPLOS:
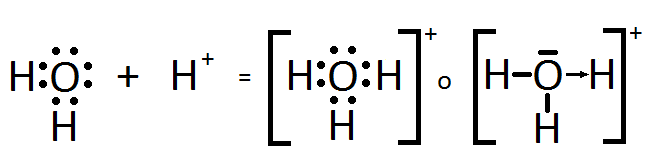
ENLACE COVALENTE COORDINADO (DATIRO)
- SE FORMA POR UN ELEMENTO CON UN PAR DE ELCTRONES , Y OTRO ALTAMENTE ELECTRONEGATIVO.
- EL PRIMERO DONA EL PAR DE ELECTRONES , QUEDANDO COMO CATION .
- EL SEGUNDO ACEPTA LOS ELECTRONES Y ATRAE AL CATION POR FUERZA ELECTROESTATICA.
- EL ENLACE ESTA FORMADO UNICAMENTE POR ELECTRONES DE DONAR(EL MENOS ELECTRONEGATIVO).
EJEMPLO:


Comentarios
Publicar un comentario